La espectrometría de masas de ionización química puede detectar con precisión compuestos orgánicos volátiles en una variedad de condiciones. Sin embargo, el análisis se vuelve ambiguo cuando el compuesto está enmascarado por una interferencia simétrica o isotrópica. Dado que no existe una medición concluyente de las estructuras que contribuyen al pico del espectro de masas, las superposiciones añaden ambigüedad a la identificación del pico.
En la química de sabores y perfumes, por ejemplo, este es un problema recurrente donde una sola fórmula molecular (ion) puede existir en múltiples isoformas. Dado que cada ion contribuye de manera diferente a cómo se percibe un sabor o una fragancia, todos son importantes.
El salicilato de metilo y el metilparabeno, que son isómeros de la vainillina, se muestran en la Figura 1. espectrometría de masas Se requiere una dimensión adicional de separación para separar y diferenciar estos isómeros.
Figura 1. Estructuras isoméricas de salicilato de metilo y metilparabeno. Crédito de la imagen: TOFWERK
La espectrometría de transferencia de iones (IMS) es un método que se puede combinar con la espectrometría de masas cuando se requiere distinguir isómeros separados. Los iones que adoptan configuraciones con diferentes secciones transversales de colisión se pueden caracterizar por espín medio (es decir, tamaño molecular medio) mediante IMS.
ionización química Se utiliza para ionizar los análisis en Enfoque IMS-MS, y los iones resultantes se separan mediante secciones transversales de colisión antes del análisis de masas. La relación masa-carga y el IMS asociado con la sección transversal se proporcionan como datos 2D. Varios componentes simultáneos o isopresivos presentes en el pico de un solo espectro de masas se desconvolucionan de esta manera.
Ejecución de Vocus CI-IMS-TOF
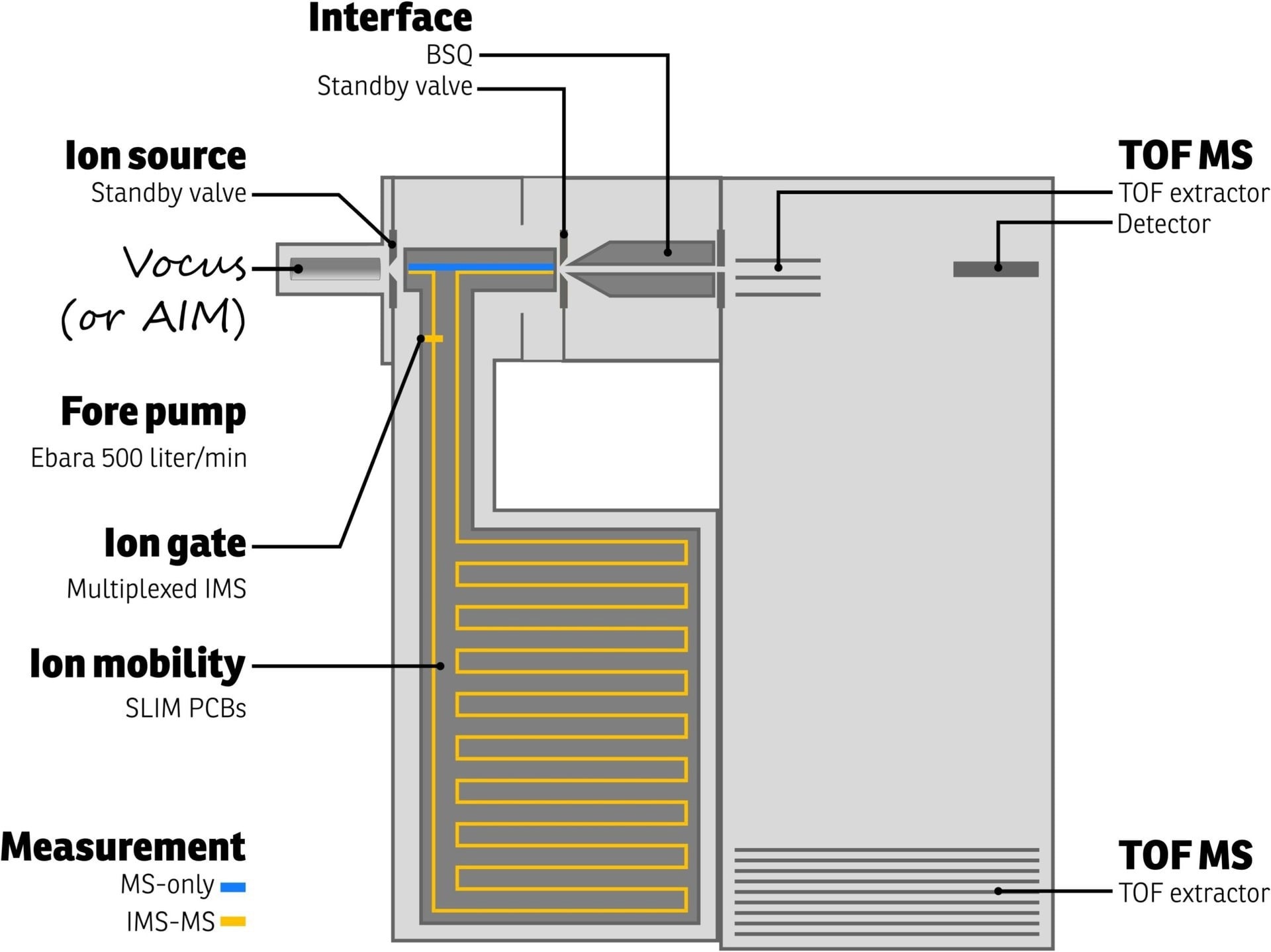
El esquema Vocus CI-IMS-TOF de TOFWERK se muestra en la Figura 2. Los iones son producidos por una fuente Vocus en este dispositivo y luego se dirigen a la cámara de separación IMS.
Figura 2. Representación esquemática del instrumento TOFWERK Focus-IMS-TOF. Las mediciones de solo MS e IMS-MS se pueden realizar como lo indican las pistas de iones azul y naranja, respectivamente. Crédito de la imagen: TOFWERK
La cámara se mantiene a una presión de 3 bar y se purga con un gas aislante inerte (como nitrógeno, helio, etc.). Usando tecnología creada en el Laboratorio Nacional del Noroeste del Pacífico para la Manipulación de Iones sin Pérdida (SLIM), los iones se transportan a lo largo de una ruta serpenteante de 9 metros de altura.1 Los campos eléctricos débiles se utilizan para regular el flujo de iones.
Los iones con secciones transversales de colisión más pequeñas experimentan menos resistencia a medida que se mueven a través del gas dieléctrico y alcanzan el final de la zona de deriva más rápido que los iones con secciones transversales de colisión más grandes. El tiempo de deriva de IMS, que está relacionado con la sección transversal de colisión de la molécula, indica el tiempo total que tarda un ion en viajar a través de la región de deriva de IMS.
TOFWERK Vocus CI-IMS-TOF proporciona dos modos de funcionamiento. El primer modo permite al usuario realizar mediciones de MS solo omitiendo el IMS (ruta azul en la Fig. 2).
El segundo modo del proceso utiliza un interruptor de iones para controlar el flujo de iones a través del IMS (ruta naranja en la Fig. 2), lo que genera datos 2D que se pueden usar para desenredar las contribuciones de diferentes isómeros o isobaras. Las capacidades TOF de Vocus CI-IMS-IMS son fáciles de operar cuando se necesitan.
Separación de isómeros con el movimiento de iones.
Es posible demostrar la separación de Vocus IMS examinando los isómeros de salicilato de metilo y metilparabeno. En la química de la reacción de transferencia de protones (PTR), estos compuestos muestran picos de espectro de masas idénticos a la misma masa de protón correspondiente (153,05 s), porque difieren solo en la posición del grupo hidroxilo en el anillo aromático.
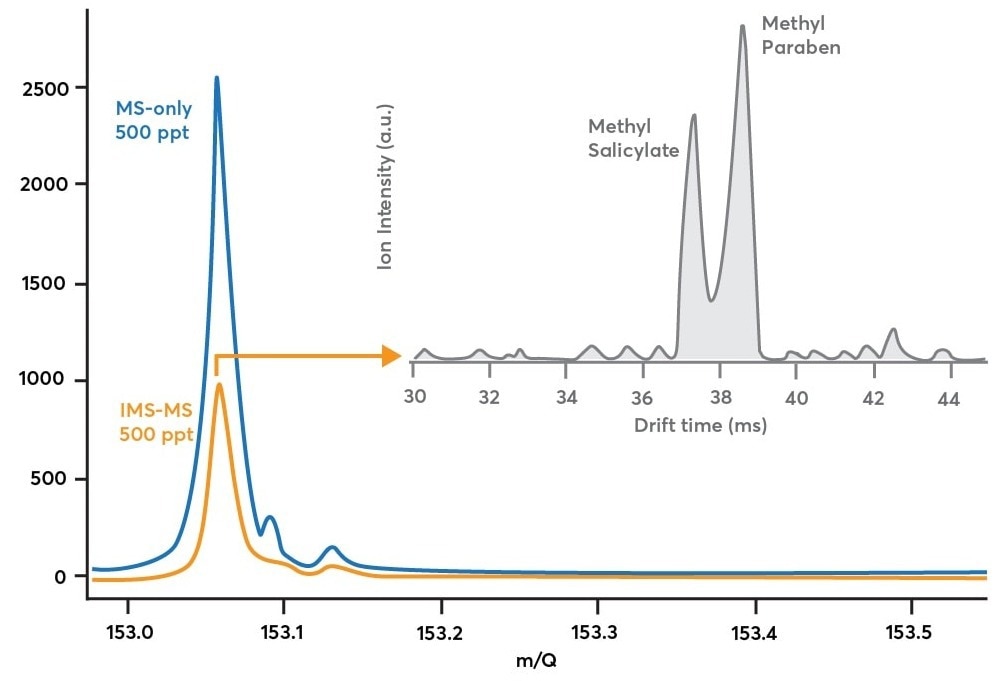
Esto se muestra experimentalmente en el trazo azul de la Fig. 3. Esta información se recopiló recolectando una mezcla de salicilato de metilo y metilparabeno en el aire en modo MS solo a concentraciones de 500 ppt (ruta azul en la Fig. 2, azul en la Fig. 3 ).
Esta información no dice cuántos isómeros contribuyeron al pico, solo aquellos con al menos un C8h8a3 El barco estaba presente. La única forma de hacerlo es activar el análisis IMS.
Figura 3. Traza azul: espectro de masas obtenido al tomar muestras de 500 partes de salicilato de metilo y 500 partes de metilparabeno solo en modo MS (pista azul en la Fig. 2). Traza naranja: el espectro de masas se adquirió mientras se muestreaba la mezcla de salicilato de metilo/metilparabeno en modo IMS (traza naranja en la Fig. 2). Traza gris: muestra cómo el espectro de masas decae en naranja a lo largo de la dimensión del movimiento de iones para revelar múltiples componentes después de 90 s de adquisición. Crédito de la imagen: TOFWERK
Los componentes característicos de un solo pico de masa se pueden distinguir debido a la activación del modo IMS. Una vez que se activa la puerta de iones, se somete a una secuencia pseudoaleatoria (múltiple), que modula la señal de los iones y proporciona datos de tiempo importantes para determinar los períodos de deriva. Luego, los iones se dirigen a la región de salto (ruta naranja en la Fig. 2).
Al comparar el espectro de masas de IMS-MS (trazo naranja) con el espectro de masas solo de MS (trazo azul) en la Fig. 3, está claro que la modificación de los iones provocó la pérdida de iones.
Teóricamente, el modo IMS-MS debería medir el 50 % de la señal iónica en comparación con el modo solo MS debido al ciclo de trabajo del 50 % de la secuencia de puerta. Se pierden pocos iones en la región de deriva o en la puerta de iones, como se muestra experimentalmente al medir el 40 % de la señal iónica en el modo IMS-MS en comparación con el modo solo MS (10 % de discrepancia entre la teoría y el experimento).
Esta compensación en la densidad de iones permite la producción de distribuciones de tiempo de deriva para una amplia gama de relaciones de masa a carga. El ciclo de trabajo aumenta al 50% con multiplexación de <1% en modos no multiplexados. El trazo gris representa la distribución del tiempo de deriva para 153.05 Th en la Fig. 3.
Esta traza, con un promedio de más de 90 segundos, demuestra la separación efectiva del salicilato de metilo del metilparabeno. Esto hace posible comprobar rápidamente la presencia de cualquiera de las dos especies y seguir la evolución de sus concentraciones relativas a lo largo del tiempo.
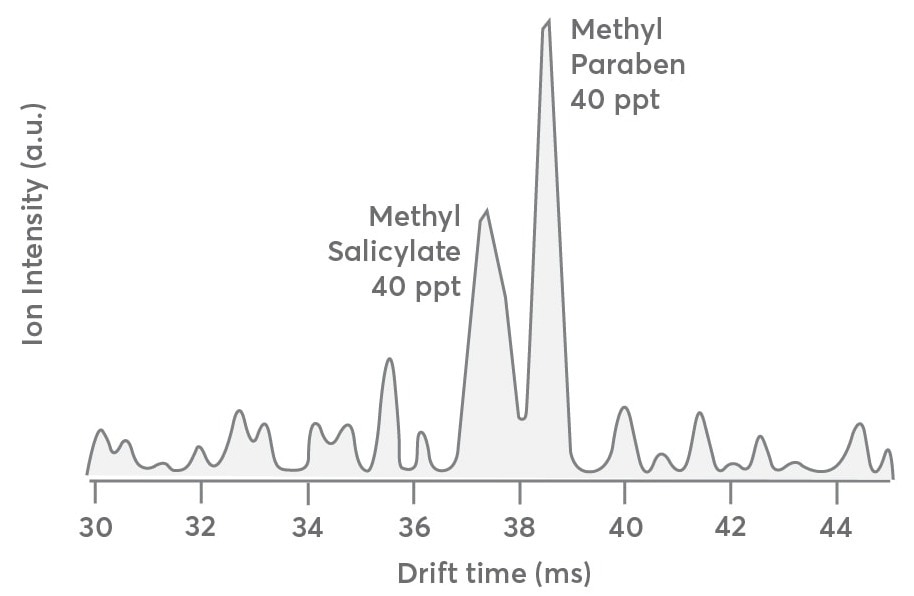
El mismo conjunto de datos que se muestra en la Fig. 3 muestra la distribución de deriva IMS del primer isótopo de carbono (13C1C7h9a3+, m/h = 154,05 w) a partir de una mezcla de salicilato de metilo y metilparabeno. Esto ayudará a los usuarios a comprender cómo la relación S:N de los datos del IMS puede disminuir en concentraciones inferiores a 500 partes por mil. Dado que sólo el 8% de 12Se espera que el padre C, o 40 partes por compuesto, esté presente en la concentración de isótopo de carbono elemental, y estos datos son informativos.
La distribución del tiempo de deriva debe ser idéntica a la distribución observada para 12Compuestos originales C en la Fig. 3 (trazo gris), además de una baja concentración. Aunque el patrón de deriva que se muestra en la Fig. 4 es cualitativamente similar al de la Fig. 3, la relación S:N empeora a medida que se acerca el LOD del instrumento.
Esto indica que el Vocus CI-IMS-MS puede separar e identificar analitos en concentraciones de hasta 40 ppm, pero requiere tiempos promedio más prolongados.
Figura 4. Distribución del tiempo de deriva del primer isótopo de carbono (13C1C7h9a3+, m/Q 154.05) de salicilato de metilo y metilparabeno muestreados a 40 ppt. El espectro es cualitativamente similar al que se muestra en la Fig. 3 excepto por la baja relación S:N. Crédito de la imagen: TOFWERK
Observación en tiempo real de la población de isómeros
Aunque los datos presentados en las Figuras 3 y 4 promediaron más de 90 ms, los tiempos de deriva típicos ocurrieron entre 20 y 150 ms. Es concebible rastrear los ensamblajes de los isómeros en tiempo real ya que las separaciones cinéticas ocurren en períodos tan cortos.
Esto es útil para los procesos con los que luchan las herramientas rápidas de cromatografía de gases, como aquellos en los que las proporciones de isómeros cambian en menos de 60 segundos.
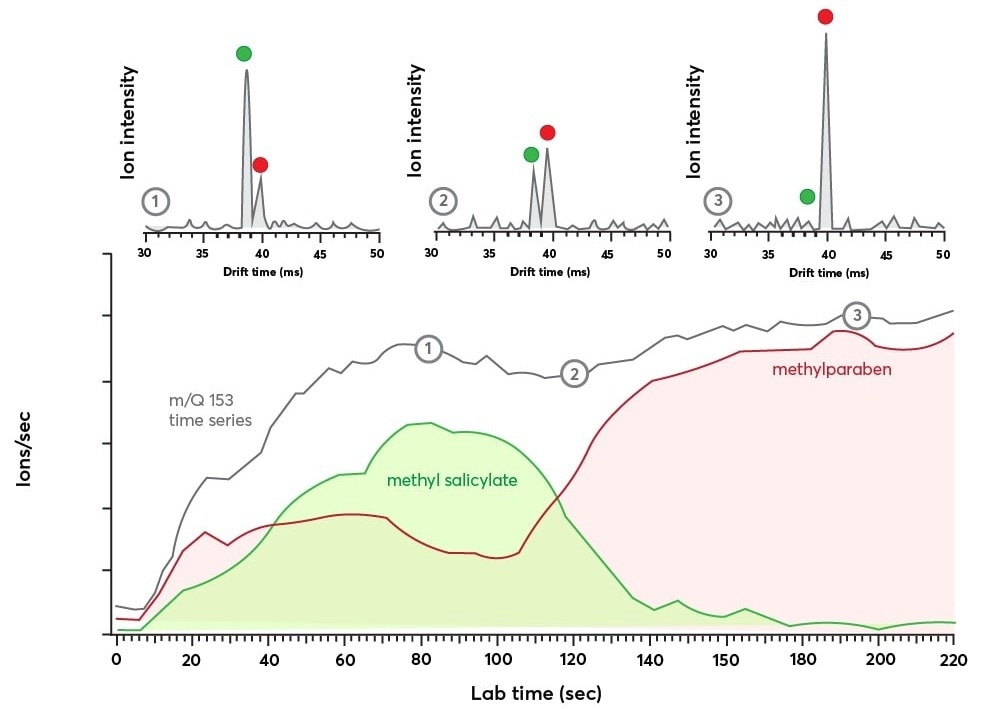
Los resultados de un experimento que muestra la detección en tiempo real de grupos de isómeros se muestran en la Figura 5. Aquí, se usa un sistema de titulación líquida (LCS) y se coloca una pequeña cantidad de una solución de salicilato de metilo. Luego se registra la respuesta del dispositivo.
En este experimento, se esperaría que la señal de salicilato de metilo aumentara inicialmente antes de comenzar a disminuir a medida que la solución de metilparabeno la elimina del sistema. Cuando la inyección de salicilato de metilo deja de diluir el metilparabeno después de la operación, la concentración más alta es de 2,5 ppb.
Figura 5. Panel inferior: datos de series temporales para m/Q = 153 Th que muestran la evolución de la corriente de iones con el tiempo (en gris). La dimensión IMS revela la respuesta trans a los isómeros de salicilato de metilo (en verde) y metilparabeno (en rojo). Panel superior: espectros IMS registrados en tres momentos diferentes durante la serie temporal m/Q = 153 Th según las Figuras 1, 2 y 3. Los espectros IMS se promediaron durante 2,9 s y muestran un claro intercambio de la población de iones de metilo salicilato a salicilato de metilo Parabeno. Crédito de la imagen: TOFWERK
En el panel superior de la Fig. 5 se muestran tres «instantáneas» del espectro IMS, cada una con un promedio de 2,9 s, desde puntos separados del experimento. Los picos de los espectros de masas relacionados con el salicilato de metilo y el metilparabeno, respectivamente, se indican mediante los puntos verde y rojo. Dado que la intensidad de estos rasgos cambia con el tiempo, esto significa que la población relativa de ambas especies también cambiará.
Al integrar las señales IMS individuales y dividir la corriente de iones observada por la relación de las regiones integradas, se pueden rastrear los cambios en los grupos de isómeros. Los resultados del uso de esta técnica para analizar las señales IMS de salicilato de metilo y metilparabeno se muestran en el panel inferior de la Figura 5.
La señal del salicilato de metilo (verde) aumenta rápidamente hasta que alcanza un pico a los 80 segundos, momento en el cual declina. La señal de metilparabeno (roja) sigue siendo débil incluso más adelante en la ejecución.
Ambos datos de series temporales para el salicilato de metilo y el metilparabeno se incluyen como contribuciones al canal m/Q Th, que se muestran en gris. Aquí, la señal aumenta rápidamente antes de estabilizarse después de unos 70 segundos.
No hay evidencia clara de que los grupos de isómeros cambien más allá de este punto. Los espectros de IMS en el panel superior se adquirieron en los tiempos indicados por las etiquetas correspondientes, que están representadas por las etiquetas «1», «2» y «3» a lo largo de la traza de la serie temporal.
Si bien es posible recopilar los datos de cromatografía de gases que se muestran en las Figuras 3 y 4, sería difícil replicar los datos en tiempo real que se muestran en la Figura 5. Para las personas que desean un análisis rápido con separación de isómeros, TOFWERK Focus CI-IMS -TOF realiza la separación de isómeros en una escala de tiempo mucho más rápida que GC.
referencia
Esta información ha sido obtenida, revisada y adaptada de materiales proporcionados por TOFWERK.
Para obtener más información sobre este recurso, visite tofwerk

«Gurú del alcohol. Analista. Defensor de la comida. Aficionado extremo al tocino. Experto total en Internet. Adicto a la cultura pop. Pionero de viajes sutilmente encantador».